iPS細胞於輸血醫學的運用與發展
編譯撰述/陳世利
往往在缺血季節與重大天災、人禍等重大災難發生時,台灣民眾總是展現出最團結與感人的精神,各地捐血車都是大排長龍,大家紛紛挽袖無償捐血救人。但是隨著醫學科技的再進步與突破,未來,這樣的排隊捐血場景也許會被改變。
大家都知道,我們都是從一顆受精卵細胞,經過不斷的細胞分裂與細胞分化後,最終成為一個個體。但是,在人體不斷新陳代謝的過程下,有些細胞會逐漸老化與凋零,這時候則需要由新形成的細胞來做交替,以維持原本的器官與組織功能。這樣的過程,幹細胞(stem cell)扮演著重要的功能。例如在發育過程中,胚胎時期各式各樣的幹細胞扮演著器官形成的重要使命;成人後,在受損的器官臟器中,成體幹細胞則負責修復與進行代謝。
由於這些幹細胞具備分化與細胞複製的能力,也成為再生醫學領域最被期待的細胞來源;除此之外,幹細胞也具備良好的增生能力,可以進行自我更新(self-renewal)。一般的體細胞,在分化之後,幾乎不再進行細胞分裂,停止細胞增生。然而,幹細胞負擔起發育與組織修補的功能,如果不具備自我增生能力,則便無法產生足量的細胞,來執行發育與修補的功能。
我們人類的幹細胞依照發育時期,常聽到的幹細胞主要可分為兩大類:發育時期中的胚胎幹細胞(Embryonic Stem cells)與成體幹細胞(Adult Stem cells)。胚胎幹細胞來自於動物或是人體發育胚胎中具有多能性分化能力之幹細胞,具備能分化成各式各樣組織器官細胞的能力。在成體中,成體幹細胞則存在於各個發育成熟的組織器官中,通常為該組織之前驅細胞。到目前為止,相關文獻上已記錄了從骨髓、腸道、皮膚、肝臟等器官之案例,這些組織均能分離出此類未分化而具有分化能力的成體幹細胞。
雖然人類胚胎幹細胞技術已被發展成功,但這項技術牽涉到人類胚胎之取得與利用,所引起之倫理爭議引起大眾的疑慮。雖然現今在美國進行人類幹細胞之研究,已經不受以往的禁令約束,但是在美國或是其他國家,對於人類胚胎幹細胞的研究仍顧慮到來源,在細胞的取得上有明確的要求和限制。因此,在醫療臨床應用或是研究上,人類胚胎幹細胞仍受到道德倫理的限制而進步遲緩;另一個主要的問題在於,現在的胚胎幹細胞株並非來自於患者本身,用於治療時,無法迴避患者本身免疫系統之攻擊與排斥。
但是如果將某些特定的遺傳基因放進從人體上提取的少量皮膚細胞中,這些皮膚細胞就會變成其他形態完全不同的細胞,並可近乎無限地增殖成長。由此誕生的細胞具有可分化為骨、心臟、神經、肝臟、血液等各種細胞、臟器的能力。這便是日本京都大學山中伸彌教授於2006年在全球率先開發出的誘導性多功能幹細胞「iPS(induced pluripotent stem cell)細胞」。
這種iPS細胞最突出的特點是幾乎可以無限增殖,並可分化成任何一種細胞;說穿了就是人工製造出可變化為其他細胞的「幹細胞」,使其增殖、分化,發育成各種細胞和臟器。這與受精卵增殖、分化形成各種細胞和臟器,或受傷後皮膚和血管進行再生的機制相同。
前文提到廣為人知的胚胎幹細胞雖同樣也是一種多功能幹細胞,但由於它是通過受精卵胚胎培育而成,因此被認為存在倫理問題。在這一點上,可由成人的體細胞(除生殖細胞外的其他細胞的總稱)培育成的iPS細胞就不存在倫理問題。
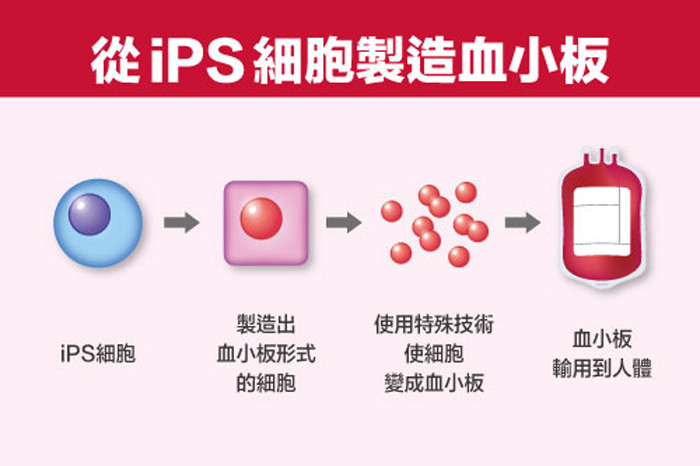
在2009年日本東京大學團隊成功利用人體皮膚細胞誘導成為iPS細胞,進而培育出少量的血小板。而京都大學iPS細胞研究所臨床應用研究部的江藤浩之教授的研究室,更利用iPS細胞培育,來開發各種血液細胞的誘導技術,最後他們成功利用iPS細胞大量生成血小板的方法。
我們都知道,血小板會在皮膚和血管受損時封閉傷口,形成瘡痂,具有抑制出血的作用;在治療血小板減少症方面,採用血小板製劑進行輸血是一種有效辦法。但是,由於血小板非常容易喪失活性,按現有技術,提取後只能保存5天,因此有些地區出現供求失衡的問題。同時,病人也會因為反覆輸血會產生抗血小板抗體,由於免疫學上的排斥反應,輸入體內的血小板甚至可能被迅速清除。
所以運用此技術來人工製造血小板,那就不必再依賴於時間冗長與有感染風險的捐血方式了。而且,如果血小板來自從患者本身的體細胞培養出的iPS細胞,那麼免疫學上的排異反應等問題也可以隨之得到解決,所以輸血醫學界目前正積極試驗,期望能在實驗室內培養大量血小板。除此之外,紅血球正是下一個利用iPS細胞技術來大量人工培養的對象。
雖然iPS細胞仍存在形成腫瘤的風險。但是,無核血小板和紅血球不會形成腫瘤,如果採用放射線照射以防止其他細胞增殖,之後再進行輸血,安全性就可得到保證。從這個意義上,也可以說借助iPS細胞在血液領域開展的研究已經相當接近臨床應用階段了。
為了能夠更加高效地利用iPS細胞,日本紅十字會等已經建立了iPS細胞庫,利用少數人的血液細胞制成iPS細胞並保存起來,可以更快捷、更廉價地開展有關移植研究與應用;在2012年山中伸彌教授也因此獲得諾貝爾生物醫學獎。
台灣推動無償捐血運動即將屆滿半世紀,在社會大眾的支持下才有今日的規模,近年各國均派員來台灣學習招募經驗、提升品質策略、高效能流程等。未來,我們也要秉持著社會公益的精神,在募血及提昇血液品質之餘,透過不間斷的學習與交流,為捐血者者做最完善的服務,更需運用各國最新的輸血醫學技術,持續為台灣醫療用血做最嚴格的把關。
編譯資料來源:
1. 株式会社メガカリオン http://www.megakaryon.com/dataroom/pdf/20170807.pdf
2. 日本時報
https://www.japantimes.co.jp/news/2017/08/07/national/science-health/worlds-first-method-mass-producing-platelets-ips-cells-unveiled-kyoto-startup/#.WxjQScsUk5u
3. http://www.megakaryon.com/technology/
4.
往往在缺血季節與重大天災、人禍等重大災難發生時,台灣民眾總是展現出最團結與感人的精神,各地捐血車都是大排長龍,大家紛紛挽袖無償捐血救人。但是隨著醫學科技的再進步與突破,未來,這樣的排隊捐血場景也許會被改變。
大家都知道,我們都是從一顆受精卵細胞,經過不斷的細胞分裂與細胞分化後,最終成為一個個體。但是,在人體不斷新陳代謝的過程下,有些細胞會逐漸老化與凋零,這時候則需要由新形成的細胞來做交替,以維持原本的器官與組織功能。這樣的過程,幹細胞(stem cell)扮演著重要的功能。例如在發育過程中,胚胎時期各式各樣的幹細胞扮演著器官形成的重要使命;成人後,在受損的器官臟器中,成體幹細胞則負責修復與進行代謝。
由於這些幹細胞具備分化與細胞複製的能力,也成為再生醫學領域最被期待的細胞來源;除此之外,幹細胞也具備良好的增生能力,可以進行自我更新(self-renewal)。一般的體細胞,在分化之後,幾乎不再進行細胞分裂,停止細胞增生。然而,幹細胞負擔起發育與組織修補的功能,如果不具備自我增生能力,則便無法產生足量的細胞,來執行發育與修補的功能。
我們人類的幹細胞依照發育時期,常聽到的幹細胞主要可分為兩大類:發育時期中的胚胎幹細胞(Embryonic Stem cells)與成體幹細胞(Adult Stem cells)。胚胎幹細胞來自於動物或是人體發育胚胎中具有多能性分化能力之幹細胞,具備能分化成各式各樣組織器官細胞的能力。在成體中,成體幹細胞則存在於各個發育成熟的組織器官中,通常為該組織之前驅細胞。到目前為止,相關文獻上已記錄了從骨髓、腸道、皮膚、肝臟等器官之案例,這些組織均能分離出此類未分化而具有分化能力的成體幹細胞。
雖然人類胚胎幹細胞技術已被發展成功,但這項技術牽涉到人類胚胎之取得與利用,所引起之倫理爭議引起大眾的疑慮。雖然現今在美國進行人類幹細胞之研究,已經不受以往的禁令約束,但是在美國或是其他國家,對於人類胚胎幹細胞的研究仍顧慮到來源,在細胞的取得上有明確的要求和限制。因此,在醫療臨床應用或是研究上,人類胚胎幹細胞仍受到道德倫理的限制而進步遲緩;另一個主要的問題在於,現在的胚胎幹細胞株並非來自於患者本身,用於治療時,無法迴避患者本身免疫系統之攻擊與排斥。
但是如果將某些特定的遺傳基因放進從人體上提取的少量皮膚細胞中,這些皮膚細胞就會變成其他形態完全不同的細胞,並可近乎無限地增殖成長。由此誕生的細胞具有可分化為骨、心臟、神經、肝臟、血液等各種細胞、臟器的能力。這便是日本京都大學山中伸彌教授於2006年在全球率先開發出的誘導性多功能幹細胞「iPS(induced pluripotent stem cell)細胞」。
這種iPS細胞最突出的特點是幾乎可以無限增殖,並可分化成任何一種細胞;說穿了就是人工製造出可變化為其他細胞的「幹細胞」,使其增殖、分化,發育成各種細胞和臟器。這與受精卵增殖、分化形成各種細胞和臟器,或受傷後皮膚和血管進行再生的機制相同。
前文提到廣為人知的胚胎幹細胞雖同樣也是一種多功能幹細胞,但由於它是通過受精卵胚胎培育而成,因此被認為存在倫理問題。在這一點上,可由成人的體細胞(除生殖細胞外的其他細胞的總稱)培育成的iPS細胞就不存在倫理問題。
在2009年日本東京大學團隊成功利用人體皮膚細胞誘導成為iPS細胞,進而培育出少量的血小板。而京都大學iPS細胞研究所臨床應用研究部的江藤浩之教授的研究室,更利用iPS細胞培育,來開發各種血液細胞的誘導技術,最後他們成功利用iPS細胞大量生成血小板的方法。
我們都知道,血小板會在皮膚和血管受損時封閉傷口,形成瘡痂,具有抑制出血的作用;在治療血小板減少症方面,採用血小板製劑進行輸血是一種有效辦法。但是,由於血小板非常容易喪失活性,按現有技術,提取後只能保存5天,因此有些地區出現供求失衡的問題。同時,病人也會因為反覆輸血會產生抗血小板抗體,由於免疫學上的排斥反應,輸入體內的血小板甚至可能被迅速清除。
所以運用此技術來人工製造血小板,那就不必再依賴於時間冗長與有感染風險的捐血方式了。而且,如果血小板來自從患者本身的體細胞培養出的iPS細胞,那麼免疫學上的排異反應等問題也可以隨之得到解決,所以輸血醫學界目前正積極試驗,期望能在實驗室內培養大量血小板。除此之外,紅血球正是下一個利用iPS細胞技術來大量人工培養的對象。

雖然iPS細胞仍存在形成腫瘤的風險。但是,無核血小板和紅血球不會形成腫瘤,如果採用放射線照射以防止其他細胞增殖,之後再進行輸血,安全性就可得到保證。從這個意義上,也可以說借助iPS細胞在血液領域開展的研究已經相當接近臨床應用階段了。
為了能夠更加高效地利用iPS細胞,日本紅十字會等已經建立了iPS細胞庫,利用少數人的血液細胞制成iPS細胞並保存起來,可以更快捷、更廉價地開展有關移植研究與應用;在2012年山中伸彌教授也因此獲得諾貝爾生物醫學獎。
台灣推動無償捐血運動即將屆滿半世紀,在社會大眾的支持下才有今日的規模,近年各國均派員來台灣學習招募經驗、提升品質策略、高效能流程等。未來,我們也要秉持著社會公益的精神,在募血及提昇血液品質之餘,透過不間斷的學習與交流,為捐血者者做最完善的服務,更需運用各國最新的輸血醫學技術,持續為台灣醫療用血做最嚴格的把關。
編譯資料來源:
1. 株式会社メガカリオン http://www.megakaryon.com/dataroom/pdf/20170807.pdf
2. 日本時報
https://www.japantimes.co.jp/news/2017/08/07/national/science-health/worlds-first-method-mass-producing-platelets-ips-cells-unveiled-kyoto-startup/#.WxjQScsUk5u
3. http://www.megakaryon.com/technology/
4.

瀏覽人數:11529
最新異動時間:2018/09/13
最新異動時間:2018/09/13
最新文章










